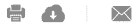Estabilidad de los medicamentos en el agua de bebida
Interacciones y reactividad
Por Joan Freixes, CENAVISA, S.L.
El agua de bebida es la vía de administración principal de medicamentos en tratamientos masivos para aves y cerdos. Por ello, será fundamental conocer el comportamiento y la estabilidad de un medicamento en el agua de bebida, en las condiciones de uso, es decir, durante el tiempo en que el agua medicada está a disposición de los animales para ser consumida.
Las etapas del ciclo de vida de un medicamento van desde su elaboraciónhasta la administración final a los animales. Precisamente, es esta última etapa uno de los puntos críticos del ciclo puede condicionar el éxito o el fracaso de un tratamiento terapéutico, de la administración de los medicamentos en el agua de bebida.
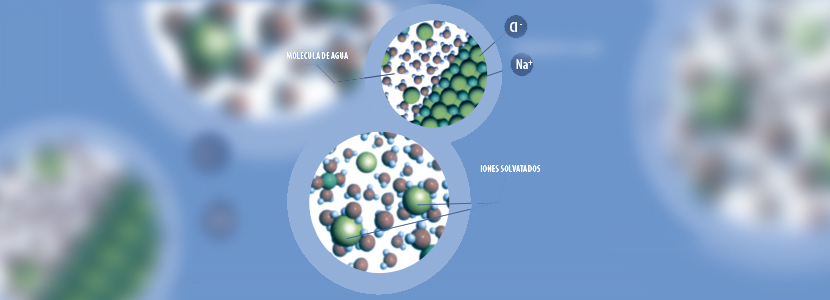
El agua es capaz de solvatar sustancias iónicas como las sales o meléculas como la glucosa a través de puentes de hidrógeno
Químicamente la molécula de agua es muy sencilla. Está constituida por dos átomos de hidrógeno y uno de oxígeno, dispuestos espacialmente como un dipolo, es decir, con la carga eléctrica repartida asimétricamente. Esta propiedad es la responsable del poder disolvente del agua, capaz de solvatar sustancias iónicas como las sales, por interacciones de tipo electrostático, o moléculas como la glucosa, por ejemplo, a través de puentes de hidrógeno.
-Antes de analizar las posibles causas que influyen en la estabilidad de un medicamento en el agua de bebida, conviene tener en cuenta una serie de consideraciones:
- Cuando el medicamento se administra en el agua a través de un dosificador, el recipiente de la solución madre o concentradose comporta como un reactor químico, donde pueden tener lugar distintos procesos químicos
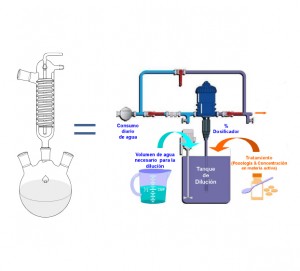
Figura 2. Dosificador de agua
- Supongamos que un fármaco A, ingrediente activo de un medicamento, se transforma en el agua en un producto de degradación B.La velocidad de transformación se rige a través de las leyes de la cinética química. Para un proceso de primer orden se cumple la fórmula de la figura 3. La velocidad de descomposición del fármaco A es proporcional a su concentración molar (moles de fármaco/L). Ello quiere decir que, a igualdad de concentración, la velocidad de degradación de un fármaco en un recipiente intermedio de 20 L será 50 veces mas rápida que en un tanque de 1.000 L.
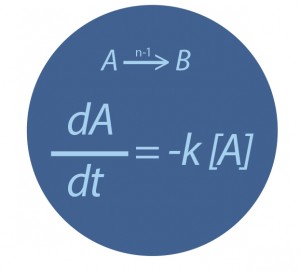
Figura 3. Leyes de la cinética química
- Un fármaco puede degradarse en el agua sin que se altere el aspecto físico de la disolución. Los cambios de coloración y la aparición de turbidez y precipitados no son los únicos indicadores de la inestabilidad de un medicamento.
“La velocidad de degradación de un fármaco será 50 veces más rápida en un recipiente de 20l que en un tanque de 1.000l”
En ocasiones se atribuye el fracaso de un tratamiento terapéutico a la falta de eficacia de los medicamentos. Sin embargo, si analizamos las posibles causas que afectan su estabilidad en el agua, nos daremos cuenta de los múltiples factores que pueden alterar un medicamento y que pueden ser la causa de la escasa respuesta terapéutica.
Cuando un medicamento está disuelto en el agua, las moléculas de los fármacos que lo componen son susceptibles de interaccionar con los elementos ambiambientales, que provocan un bombardeo constante que altera su estructura química, como resultado de diferentes reacciones de transformación.
- Hidrólisis: reacción con el agua
- Oxidación: reacción con el oxígeno atmosférico
- Fotólisis. Fragmentación o transformación de una molécula por absorción de energía radiante
- Isomerización (epimerización): formación de isómeros ópticos menos activos
- Formación de complejos de coordinación con iones Ca2+ y Mg2+
- Polimerización: reacción de una molécula con sus productos de degradación primarios
Figura 4. Acción de los agentes ambientales sobre los fármacos disueltos.
Factores que pueden alterar la estabilidad de un medicamento en el agua
- Dureza total (contenido por litro de iones Ca2+ y Mg2+)
Algunos fármacos reaccionan con estos iones para formar complejos de coordinación insolubles. A continuación se describen distintos ejemplos.
-El enrofloxacino es una fluoroquinolona ampliamente utilizada en avicultura. Disuelto en aguas muy duras, interacciona con los iones divalentes Ca2+ y Mg2+ formando complejos de coordinación insolubles,por cesión de pares de electrones de los átomos de oxígeno de los grupos carboxilo del enrofloxacino a orbitales d vacíos del ión Ca2+.
–Dr. SUMANO comprobó como disminuía la absorción del enrofloxacino administrado a pollos por vía oral en el agua de bebida a medida que aumentaba la dureza total del agua. Se encontraron diferencias estadísticamente significativas en la concentración sérica máxima (Csmax), en el área bajo la curva (AUC) y en la semivida de eliminación, con valores de 3.51 µg/ml, 26.21 y 0.072, respectivamente, en aguas blandas (16.5 ppm CaCO3) y 2.22 µg/ml, 13.58 y 0.069 en aguas duras (195 ppm CaCO3). La biodisponibilidad del fármaco enrofloxacino se redujo drásticamente en aguas duras un 50%.
Para leer el artículo completo haga click aquí o visite www.avicultura.info